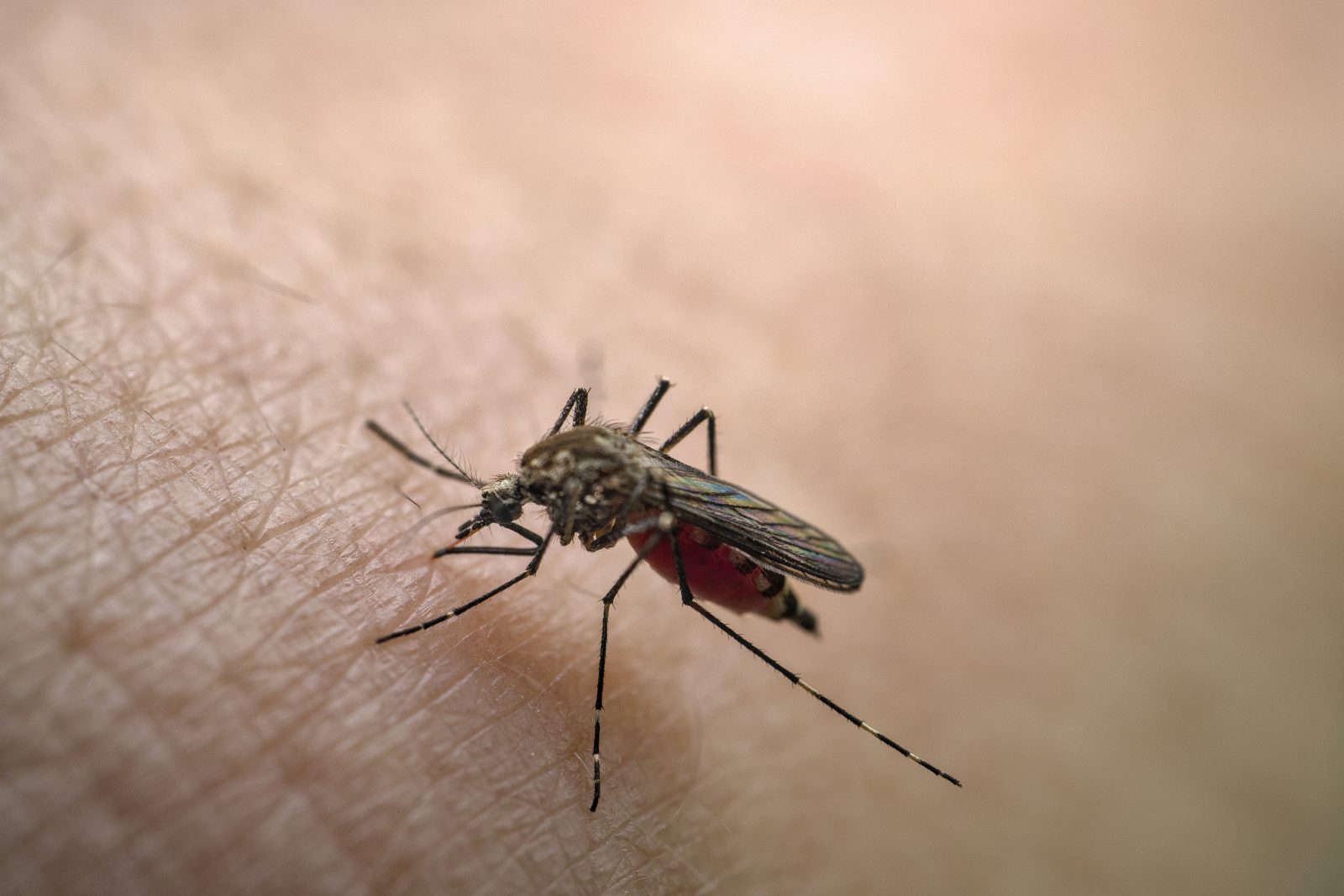
L’expérimentation animale est-elle encore pertinente ? L’exemple de la maladie de Parkinson
L'expérimentation animale fait débat. La recherche scientifique est-elle prête à se passer des animaux ? Les alternatives sont-elles suffisantes ?

**L’expérimentation animale fait débat. La recherche scientifique est-elle prête à se passer des animaux ? Les alternatives sont-elles suffisantes ? La discussion mérite en tout cas d’être menée de la manière la plus objective possible.
**
La maladie de Parkinson touche plus de 270 000 personnes en France. Lorsque le diagnostic est posé, la destruction des neurones producteurs de dopamine est trop avancée pour envisager des traitements curatifs. Pour obtenir des marqueurs précoces de la maladie, et permettre des traitements préventifs, l’équipe des chercheurs du Professeur Boulet du Grenoble Institut des Neurosciences a développé une recherche métabolomique par Résonance Magnétique Nucléaire.
A l’image de l’analyse des gaz d’échappement d’une voiture lors d’un contrôle technique dont la recherche des produits de combustion permet de déceler d’éventuelles anomalies de fonctionnement du moteur, la métabolomique par Résonance Magnétique Nucléaire permet l’identification de toutes les substances organiques de petites tailles (comme certains acides aminés) ou de leurs produits de dégradation issus des cascades des évènements moléculaires se produisant dans les cellules. L’identification de ces substances ou métabolites au sein d’un échantillon biologique, comme le sang ou d’autres tissus, permet donc de déceler d’éventuels marqueurs de la maladie (biomarqueurs). Cette approche se situe en aval de l’étude des gènes (génomique), de l’ensemble des ARN messagers (transcriptomique) et de l’ensemble des protéines (protéomique). Cette approche novatrice permet donc d’appréhender l’ensemble des facteurs (génétiques, environnementaux, nutritionnels…) dont la résultante est susceptible de conduire à une maladie.
Les chercheurs ont croisé les métabolites issus de trois modèles animaux complémentaires de la maladie de Parkinson et ont soumis aux mêmes analyses des échantillons de sang issus de patients nouvellement diagnostiqués mais non encore traités (patients de novo).
Des modèles animaux complémentaires
En 1959 les biologistes William Russel et Rex Burch ont proposé des recommandations éthiques en expérimentation animale connues sous le terme de « règle des 3 R » qui font encore aujourd’hui consensus à l’égard du traitement éthique des animaux de laboratoire. Ces recommandations visent à remplacer quand cela est possible l’utilisation d’animaux par des modèles alternatifs, réduire le nombre d’animaux requis et raffiner les expérimentations en minimisant les contraintes imposées aux animaux (douleur, souffrance, angoisse…).
Il semble contraire au critère de réduction de faire appel à une multiplicité de modèles animaux différents pour une même étude. Dans cette étude, utiliser trois modèles a permis de recouper entre elles les données, et d’en augmenter la portée « translationnelle » des résultats, c’est-à-dire ce qui permet de les transposer à l’humain. En effet, chaque modèle présentait des caractéristiques complémentaires de la maladie de Parkinson, chacun imitant différentes phases de la maladie, depuis la phase où seuls des déficits de motivation sont présents, jusqu’à celle avec des symptômes moteurs. De plus, les chercheurs ont développé une échelle de cotation de la progression de la maladie calquée sur ce qui existe en clinique humaine, évaluant les performances motivationnelles, motrices et l’étendue des lésions neurologiques. Cela a amélioré l’aspect translationnel de ces études et a participé aussi au raffinement des expérimentations.
Le premier modèle porte sur des rats traités par une neurotoxine ciblant les neurones dopaminergiques. Il est ainsi possible de constituer des lots d’animaux mimant de façon stable et sans évolution temporelle, un stade précis de la maladie ; ceci est une simplification de la maladie humaine où chaque patient est un cas particulier évolutif. En complément, les chercheurs ont sélectionné un second modèle reflétant la nature progressive de la pathologie dont le marqueur est lié à la production d’une protéine délétère. Bien que ce modèle permette chez un même animal de suivre la progression de la pathologie, il n’englobe pas tous les symptômes neuropsychiatriques caractéristiques du stade précoce de la maladie (tel que l’apathie).
Enfin, le troisième modèle, induit par injection d’une neurotoxine à des macaques, reproduit l’évolution des phases cliniques de la maladie et présente une plus grande homologie avec l’humain. L’homologie d’un modèle se réfère à sa capacité à mimer les mécanismes physiologiques sous-jacents à l’origine de la pathologie étudiée chez l’humain : on parle donc d’identité de causalité et de mécanismes mis en jeu.
De l’animal à l’humain
Chez ces animaux, les dérégulations métaboliques ont amené à identifier six métabolites, potentiellement liés au processus neurodégénératif, dont les niveaux combinés constituent un biomarqueur métabolique composite. Ce biomarqueur permet de discriminer les animaux imitant la maladie de Parkinson des témoins, et ce, dès la phase précoce. Ce résultat n’aurait pas été atteint si une seule situation, un seul modèle animal, avait été étudié.
Les résultats obtenus chez les animaux ont ensuite été comparés avec les résultats de patients de novo (diagnostiqués mais non encore traités) provenant de deux banques différentes. Les mêmes six métabolites constituant le biomarqueur identifié chez les animaux ont permis de distinguer les patients de novo des patients sains avec un niveau élevé de sensibilité et de spécificité.
Les chercheurs ont également montré que la dérégulation de 3 des 6 métabolites composant le biomarqueur peut être partiellement corrigée par un médicament mimant les effets de la dopamine. Ce traitement permet de corriger le déficit de motivation des animaux à la phase précoce. Cette amélioration partielle a également été observée dans un sous-ensemble des patients de l’étude. Cela renforce l’intérêt du biomarqueur identifié et suggère que ce marqueur permettrait de surveiller l’évolution des traitements d’une manière moins contraignante que les méthodes d’imagerie médicale actuelles.
Outre les perspectives diagnostiques de cette étude, ces travaux ont également permis d’identifier un mécanisme de régulation du métabolisme cellulaire sur lequel on pourrait agir pour contrer les effets de la maladie, offrant ainsi des perspectives thérapeutiques. Ceci illustre notamment à quel point recherche fondamentale et recherche appliquée sont fortement indissociables l’une de l’autre. Nous venons de le voir au travers de cet exemple, mais de nombreuses recherches montrent l’intérêt de l’expérimentation animale, comme dans le cas des travaux de Pasteur sur la rage, les travaux grenoblois sur les approches par stimulations électriques intracérébrales profondes qui ont permis de révolutionner la prise en charge de nombreux patients parkinsoniens à travers le monde, ou encore, plus proche de nous, les travaux sur les ARN messagers ayant permis la mise au point de vaccins contre la Covid-19 et ont valu à leurs auteurs le prix Nobel de Médecine 2023.
Que penser de la transposabilité ?
Au-delà de ces avancées scientifiques, les détracteurs de l’expérimentation animale mettent en avant la faible transposabilité des résultats obtenus chez l’animal à l’homme, un de leurs argument étant que « 90 % des traitements testés avec succès sur les animaux se révèlent inefficaces ou dangereux pour les êtres humains ». Ceci leur permet notamment de justifier le recours à l’utilisation de modèles alternatifs à l’animal, tels que des modèles in vitro ou in silico.
Cette citation nous semble cependant partielle et partiale. Il n’a pas été démontré que la transposabilité des tests in vitro et/ou in silico soit meilleure en l’état actuel des techniques.
En réalité, ces tests sont les premiers cribles de l’ensemble des tests précliniques et la contribution des animaux est essentielle puisqu’en fin de phase pré-clinique, ils permettent d’exclure 40 % de candidats médicaments, notamment sur la base de risques potentiels chez l’humain.
Par ailleurs, les auteurs dutexte cité après avoir souligné cette faible transposabilité, proposent plutôt de mettre l’accent sur la robustesse des approches expérimentales, en assurant une recherche rigoureuse tant sur les animaux que chez les humains. Ils suggèrent ainsi « d’harmoniser la conception des protocoles expérimentaux menés chez l’humain (étude clinique) avec celle des études précliniques réalisées chez l’animal dont l’utilisation demeure indispensable, balayant la vision manichéenne qui voudrait que s’opposent une communauté pro-expérimentation animale et une autre, pro-méthodes alternatives. »
Le fait d’attribuer des capacités cognitives à l’autre – humain comme animal – nous confère un socle commun de droits moraux et apporte du sens à nos actions. Le domaine de l’expérimentation animale n’échappe pas à cette règle.
Il a été avancé que les chercheurs utilisant des animaux à des fins scientifiques auraient une moindre empathie vis-à-vis de la souffrance animale que le reste de la population.
Cette observation nous parait occulter un point important. De même qu’un chirurgien ne s’évanouit pas à la vue du sang au moment crucial de son intervention, en tant que chercheurs travaillant sur des modèles animaux, nous réfléchissons aux conséquences de nos actes. Leur aspect émotionnel est maîtrisé, mais non oblitéré : le chercheur n’a aucun intérêt à négliger la souffrance animale. Une expérience sur un modèle animal perd de sa puissance de déduction si certains animaux sont en panique, d’autres en stress, ou en prostration. Bien au contraire, la qualité de la science dans ce domaine va de pair avec le bien-être des animaux. La démarche de raffinement citée plus haut vise également à limiter les symptômes au strict minimum pour l’étude de la maladie, et elle est indissociable d’une empathie raisonnée avec les animaux utilisés.
Il est nécessaire également de rappeler que la qualité de nos avancées médicales comme de nos services de soins assume que le nombre moyen d’animaux que chaque Français « utilisera » au cours de sa vie entière est de 2,6 animaux. Ce nombre est à mettre lui-même en rapport avec les 1298 animaux, en moyenne, que pour toute sa vie un(e) Français(e) utilisera pour se nourrir. L’utilisation d’animaux en recherche expérimentale telle qu’elle est pratiquée de nos jours dans un cadre raisonné et contrôlé, et dans le respect du bien-être animal, reste, selon nous, une nécessité pour l’évolution de nos connaissances, même si son bannissement « à terme » tel qu’inscrit dans le marbre de la loi européenne doit nous inciter à en limiter le nombre et à développer des alternatives.
Enfin, en ce qui concerne le respect effectif des lois relatives à l’utilisation d’animaux en recherche, dont l’obligation d’appliquer les 3R, les inspecteurs vétérinaires départementaux ont à leur disposition des sanctions dissuasives qui peuvent être lourdes en cas de maltraitance.
En tant que chercheurs, nous savons que la recherche en expérimentation animale est sujette à des controverses : nos détracteurs adhèrent aux idées développées par les mouvements opposés à l’expérimentation animale en partie parce qu’il n’y a pas de manifestation de ceux qui sont en faveur de cette pratique. C’est précisément pour cela qu’il nous incombe de rendre compte à nos concitoyens de ce que nous faisons dans nos laboratoires.![]()
Colin Deransart a reçu des financements de la Ligue Française Contre les Epilepsies, des Laboratoires GlaxoSmithKline, de la Fondation Electricité de France, de l'ANR et d'un Programme Hospitalier de Recherche Clinique.
Bertrand Favier est membre de l'AFSTAL. Sa recherche actuelle est financée par l'ANR et la Société Française de Rhumatologie en plus de son employeur.
Boulet sabrina a reçu des financements de l'ANR, la Fondation de France, la fondation pour la Rechercher sur le Cerveau, la fondation France Parkinson.
Véronique Coizet a reçu des financements de l'ANR, la fondation France Parkinson, la Fondation de France. Elle est présidente du comité d'éthique de l'Institut des Neurosciences de Grenoble et membre du comité Santé et bien-être des animaux.











![[TRIBUNE] À ceux qui veulent travailler, l’État dit : « Restez chez vous ! »](https://media.bvoltaire.fr/file/Bvoltaire/2025/04/ddp-cceg6jpl19m-unsplash-616x411.jpg?#)
























/2022/07/12/phpe5RrYs.jpg?#)


/2025/04/28/halleberry-680f9bcf605ef261708096.jpg?#)
/2025/04/28/000-43a37np-680b6d84e0a22012872781-680fa41dac56b073669967.jpg?#)
/2025/04/28/nicolekidmanafp-680fa2d7614a7694229238.jpg?#)